Rigenerare il timo
Il nostro corpo ha bisogno di un sistema immunitario che combatta le infezioni durante il corso della vita. Il timo ha un ruolo importante all’interno del sistema immunitario, ma durante il normale processo di invecchiamento diventa più piccolo e meno efficace e può essere danneggiato anche a seguito di alcuni trattamenti medici. Come potrebbe aiutarci la ricerca sulle cellule staminali nel rimpiazzare un timo perduto o danneggiato, e quando potrebbe questo essere utile?
Il nostro sistema immunitario combatte le infezioni attraverso alcuni globuli bianchi del sangue chiamati “cellule T”, che sono prodotte in un organo chiamato timo. Il timo è quindi essenziale per avere un sistema immunitario sano.
Invecchiando, il timo degenera - diventando più piccolo e meno efficiente nel produrre le cellule T necessarie a combattere le infezioni. Attualmente ci sono poche terapie disponibili per migliorare o ristorare la funzione del timo.
Tuttavia, se gli scienziati fossero in grado di rigenerare il timo, questo potrebbe aiutare a migliorare il sistema immunitario e portare a trattamenti per diverse condizioni patologiche che colpiscono il timo, come la Sindrome di DiGeorge.
Visto quanto il timo è essenziale per un sistema immunitario sano, gli scienziati stanno attualmente cercando di capire come utilizzare le cellule staminali per riparare e rigenerare questo organo.
Gli scienziati hanno dimostrato che quando si prendono delle “cellule progenitrici” del timo (cellule simili alle staminali) da un topo e si trapiantano in un altro topo privo di timo, queste riescono a formare un timo perfettamente funzionante.
Attualmente, i ricercatori stanno studiando:
Come produrre artificialmente in laboratorio i tessuti del timo da trapiantare
Metodi per indurre il timo a auto-rigenerarsi in seguito a danno o degenerazione dovuta all'età.
Molta della ricerca attuale finalizzata all’uso delle cellule staminali come potenziale strumento per rigenerare e riparare il timo, è stata condotta nei topi. Una grossa sfida per gli scienziati è scoprire se questi risultati funzionino anche per gli umani. Ad esempio, prima che gli scienziati possano testare se una cellula umana progenitrice del timo possa dare origine ad un timo funzionale quando trapiantata, si dovrà prima capire come crescere cellule progenitrici del timo in laboratorio, e come produrne in numeri sufficienti per il trapianto.
Il timo
Il timo è l’organo dove viene prodotto un tipo specifico di globuli bianchi, noti come cellule T. Senza cellule T, non siamo protetti dalle infezioni, e non possiamo controllare in modo efficiente le cellule anormali, come le cellule del cancro.
Il normale processo di invecchiamento porta il timo a rimpicciolirsi e può subire danni in seguito a condizioni genetiche, infezioni croniche e alcune procedure mediche.
Se il timo non funziona correttamente ciò può risultare nella produzione di un numero insufficiente di cellule T, condizione chiamata immunodeficienza, o produrre cellule T che attaccano i nostri stessi corpi - condizione chiamata autoimmunità.
La condizione genetica detta Sindrome di DiGeorge è caratterizzata da riduzione o assenza del timo con rischio di gravi malattie da immunodeficienza e autoimmuni. Alcuni trattamenti medici inoltre possono danneggiare il timo come effetto collaterale. Ad esempio, la chemioterapia e la radioterapia, trattamenti comuni per la cura dei tumori del sangue come la leucemia e il linfoma, non solo riducono le cellule T mature, ma danneggiano inoltre gravemente il timo. Ripristinare la funzione del timo è necessario per produrre nuove cellule T in seguito ai trapianti di midollo osseo e ciò avviene con ritardo in alcuni pazienti. Questo ritardo è stato associato con un maggiore rischio di infezione e scarso risultato clinico.
Ci sono poche terapie clinicamente provate disponibili per migliorare o ripristinare la funzione del timo, ma ci sono numerose direzioni di ricerca:
Una terapia attuale e’ il trapianto di timo, che può sopperire alla mancanza genetica del timo come nella sindrome di DiGeorge. Tuttavia, questo trattamento e’ solo appropriato per pazienti senza timo o cellule T, poiché le cellule T del paziente stesso attaccherebbero e rigetterebbero il trapianto. Attualmente solo frammenti di timo, ottenuti da tessuto in eccesso nelle operazioni al cuore di pazienti molto giovani, possono essere utilizzati per il trapianto.
Una proteina detta “Interleuchina-22” può aiutare un timo danneggiato da chemio o radioterapia a recuperare. Esiste un test clinico in fase II che sta esaminando l’uso di questa proteina come terapia nei casi rigetto del trapianto di midollo osseo. La conta del numero di nuove cellule T in seguito al trattamento, ci rivelerà se questa proteina potrà essere usata come trattamento per aumentare la funzione del timo.
Un’altra proteina detta “Interleuchina-7” ha mostrato risultati molto promettenti nel promuovere rigenerazione immunitaria in molti modelli pre-clinici, e nell’aumentare i numeri di cellule T negli studi clinici. Negli umani, i suoi effetti diretti sul recupero del timo devono ancora essere investigati.
Alcuni risultati incoraggianti vengono da molti studi clinici i quali mostrano che l’uso dell’ormone della crescita umano aumenta il recupero del timo.
Studi pre-clinici e clinici hanno mostrato che inibire la produzione degli ormoni sessuali steroidei, chimicamente o chirurgicamente, promuove la crescita del timo e risulta in una maggiore produzione di cellule T.
I ricercatori hanno trovato delle cellule staminali o progenitrici (simili alle staminali) nel timo dei topi, le quali sono in grado di rigenerare un timo funzionale quando trapiantate. La ricerca sta anche cercando delle strategie per incoraggiare una migliore rigenerazione del timo nativo (nel corpo), e per costruire artificialmente il tessuto del timo destinato al trapianto. Ci sono diverse fonti di cellule staminali e approcci che sono in fase di studio:
1. Usare le cellule staminali del tessuto
Quando le cellule del timo di un topo sono trapiantate in un altro topo, queste generano un timo funzionale che può produrre cellule T. È necessario più lavoro per scoprire se questo succede anche nel caso delle cellule progenitrici del timo umano. Inoltre, prima che questo approccio possa essere utile clinicamente, gli scienziati devono capire come crescere le cellule staminali del timo in laboratorio per produrne le quantità necessarie per un trapianto.
2. Usare le cellule staminali pluripotenti
I ricercatori sono riusciti a produrre in laboratorio cellule simili a quelle del timo a partire dalle cellule staminali pluripotenti umane e di topo. Se questi risultati verranno migliorati affinché le cellule prodotte in laboratorio diventino identiche alle cellule del timo del corpo, questo aprirà la strada per produrre in laboratorio il tessuto del timo umano destinato al trapianto. Generare le cellule staminali pluripotenti indotte dalle cellule del paziente stesso, per poi usarle al fine di derivare da esse le cellule del timo, potrebbe essere un modo per superare l’ostacolo del rigetto immunitario.
3. Riprogrammare cellule di altri tessuti
I ricercatori sono riusciti a generare cellule umane ‘pre-T’ (le cellule che produrranno e diventeranno cellule T) a partire da cellule progenitrici del sangue umano in laboratorio. Il trapianto di queste cellule nei topi ha mostrato risultati promettenti nell’accelerare il recupero del sistema immunitario in seguito a trapianto di midollo osseo.
Le cellule pre-T sono trapiantate in parallelo alla normale terapia, in modo da maturare in cellule T all’interno del corpo del paziente stesso.
La ricerca attuale ha trovato un modo di convertire le cellule del tessuto connettivo, dette fibroblasti, in cellule progenitrici del timo in laboratorio, in un processo detto riprogrammazione. Quando queste cellule vengono trapiantate nei topi generano un timo funzionante e supportano la normale produzione di cellule T. Se questo approccio risultasse efficace anche per cellule umane, le cellule ottenute in laboratorio potrebbero essere una fonte alternativa di cellule per i trapianti di timo. Gli scienziati stanno anche usando le cellule del timo generate in laboratorio per studiare la funzione dell’organo e testare metodologie migliori per produrre un timo, o mini-timo (detto organoide) in laboratorio, che potrebbe essere utilizzato per trapianti e per testare nuovi farmaci.
Si spera che con ulteriore tempo e risorse, i ricercatori sviluppino strategie per ristorare la funzione del timo e aiutare vari pazienti.
Per la prima volta, gli scienziati hanno cresciuto un organo complesso e perfettamente funzionante trapiantando, in un animale, cellule che erano state originariamente create in laboratorio. Il team ha creato un timo - un organo nel corpo situato accanto al cuore che produce cellule immunitarie dette cellule T, vitali per la salvaguardia dalle malattie. Questo progresso potrebbe in futuro aiutare lo sviluppo di organi di sostituzione “cresciuti in laboratorio”.
- Scheda informativa di EuroStemCell sulla riprogrammazione cellulare: http://www.eurostemcell.org/it/identita-cellulare-e-riprogrammazione
- Scheda informativa di EuroStemCell sulle cellule staminali pluripotenti indotte: http://www.eurostemcell.org/it/cellule-ips-e-riprogrammazione-trasformare-ogni-cellula-del-corpo-una-cellula-staminale
- Che cosa è il timo? http://www.focus.it/scienza/salute/che-cose-il-timo
- THYMISTEM studia terapie con cellule staminali per i sistemi immunitari danneggiati: http://cordis.europa.eu/news/rcn/36463_it.html
- Primo organo rigenerato da cellule riprogrammate: http://www.ansamed.info/scienza/notizie/rubriche/biotech/2014/08/25/primo-organo-rigenerato-da-staminali-riprogrammate_0684e4b9-1a1e-4309-8918-06528d4d994c.html
- Your amazing immune system interactive book http://www.interactive-immunity.net/
- 3D map showing the location of the thymus in humans http://www.healthline.com/human-body-maps/thymus
- Thymistem – EU funded research partnership using stem cell research to develop therapys for boosting the immune system http://www.thymistem.org/our-work
Questa scheda informativa è stata creata da Amanda Holland, Emma Kemp, Cathy Southworth e Amy Hansen, e revisionata da Clare Blackburn e Marcel R.M. van den Brink.
Tradotta in italiano da Benedetta Carbone e Antonella Fidanza.
Immagini e video
(Copyright in possesso della persona menzionata a meno che non sia diversamente specificato)
Illustrazione che mostra la posizione del timo nel corpo humano © Cameron Duguid (CC BY 3.0)
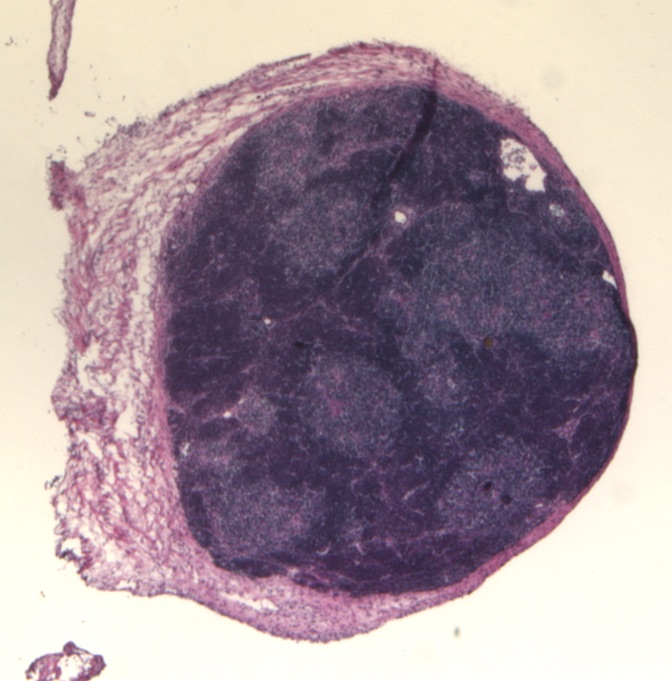
Organoidi di timo marcati con la colorazione ematossilina eosina © Nick Bredenkamp
Animazione “dentro il timo” che descrive la funzione del timo © Cameron Duguid, Clare Blackburn, Emma Kemp, Cathy Southworth and Paul Rouse. (CC BY 3.0)
Video del timo cresciuto in laboratorio che descrive come il lab di Clare Blackburn ha cresciuto il timo in laboratorio © Medical Research Council