Esplora le Cellule Staminali
In questa sezione forniamo un'introduzione alle cellule staminali, ai loro utilizzi, alla ricerca, alle schede informative, alle politiche in materia, alle news ed altri argomenti collegati.
Se non sai bene da dove iniziare, ti consigliamo di dare una occhiata alle schede informative.

Diabete: come possono essere di aiuto le cellule staminali?
• Risorsa di EuroStemCell
Le cellule staminali del cordone ombelicale: gli attuali utilizzi e le sfide future
• Risorsa di EuroStemCell
La ricerca sulle cellule staminali embrionali: un dilemma etico
• Risorsa di EuroStemCell
Rigenerazione: cosa significa e come avviene?
• Risorsa di EuroStemCell
Etica e riprogrammazione: questioni etiche dopo la scoperta delle cellule iPS
• Risorsa di EuroStemCell
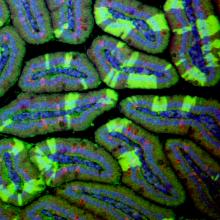
Sindrome dell’Intestino Corto: come possono aiutarci le cellule staminali?
• Risorsa di EuroStemCell
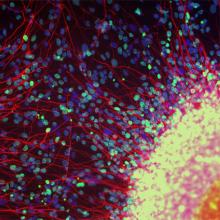
Malattia dei motoneuroni: come possono le cellule staminali aiutare?
• Risorsa di EuroStemCell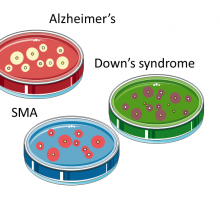
Nuovi strumenti per la ricerca medica: cellule riprogrammate come modello di patologie
• Risorsa di EuroStemCell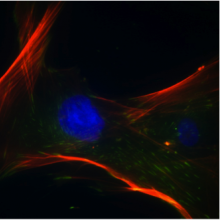
Le cellule staminali mesenchimali: le ‘altre’ cellule del midollo osseo
• Risorsa di EuroStemCell
Le cellule staminali polmonari in salute, riparazione e malattia
• Risorsa di EuroStemCell
Identità cellulare e riprogrammazione
• Risorsa di EuroStemCell
Cellule iPS e riprogrammazione: trasformare ogni cellula del corpo in una cellula staminale
• Risorsa di EuroStemCell
Distrofia muscolare: come possono aiutare le cellule staminali?
• Risorsa di EuroStemCell
Le cellule staminali del sangue: pioniere della ricerca sulle cellule staminali
• Risorsa di EuroStemCell