Neue Hilfsmittel zur Erforschung von Krankheiten: Umprogrammierte Zellen zur Modellierung von Krankheiten
Um Erkrankungen zu verstehen und erfolgreich zu bekämpfen muss Forschung betrieben werden. Jedoch wird diese oft durch eingeschränkten Zugang zu Patienten oder dem fehlenden Vorhandensein von erkranktem Gewebe, erschwert oder unmöglich gemacht. ,Krankheitsmodelle' können diese Probleme umgehen indem sie Wissenschaftlern ermöglicht Krankheiten im Labor zu überwachen. Stammzellen, besonders sogenannte induzierte pluripotente Stammzellen (,iPS’-Zellen), ermöglichen es Wissenschaftlern Krankheiten, für die es bisher kaum Studienmaterial gab, im Labor zu modellieren und daraus neue Erkenntnisse zu gewinnen.
Was wissen wir? ▼
Forscher erschaffen iPS-Zellen, indem sie spezialisierte adulte Zellen wie z. B. Hautzellen „umprogrammieren“. Aus den iPS kann dann jeder beliebige im Körper vorkommende Zelltyp wie Herz- oder Gehirnzellen hergestellt werden.
Da iPS-Zellen über dieselben Gene und Mutationen wie die Patienten verfügen, von denen sie stammen, können die Forscher iPS-Zellen nutzen, um Krankheiten im Labor nachzubilden und zu erforschen, wie die Genetik des Patienten zu dieser Krankheit beiträgt.
Mit iPS-Zellen können Forscher die „Zelldifferenzierung“, den Prozess der Spezialisierung einer Zelle, beobachten und sehen, was während der Differenzierung schief gehen kann und dann zu verschiedenen Krankheiten führt.
Was untersuchen Forscher? ▼
Viele Krankheiten werden nun an iPS-Modellsystemen studiert. Dies reicht von neurologischen Erkrankungen wie amyotropher Lateralsklerose (ALS) bis zu Bluterkrankungen und Immundefekten.
iPS-Zellen werden zur Produktion von erkrankten Zellen verwendet, an denen neue Arzneimittel und Behandlungen im Labor getestet werden.
Die Forscher verwenden iPS-Zellen, um an den Zellen des Patienten ‘die Zeit zurückzudrehen’ und zu beobachten, wie gesunde Zellen erkranken. iPS-Zellen lassen die Wissenschaftler auch untersuchen, wie die Gene, Mutationen und Umweltbedingungen eines Patienten das Fortschreiten der Erkrankung beeinflussen könnten.
Was sind die Herausforderungen? ▼
Die Forscher lernen derzeit über iPS-Zellen noch ständig dazu. Theoretisch kann aus iPS-Zellen jeder beliebige im Körper vorkommende Zelltyp entstehen. Doch die Forscher müssen zunächst lernen, wie sie die Zellen dazu bringen, sich zu verwandeln.
Obwohl den Forschern mit den iPS-Zellen zur Verfügung stehen, welche die Gene und Mutationen zu einer Krankheit enthalten, bedeutet dies noch lange nicht, dass sich die aus diesen iPS-Zellen hervorgegangenen spezialisierten Zellen im Labor so verhalten wie erkrankte Zellen im Körper.
Die Modellierung komplexer Erkrankungen (z. B. solcher Krankheiten, die durch Probleme zwischen Zellen verursacht werden, aus denen komplexe Strukturen, Gewebe und Organe bestehen) mit iPS-Zellen ist derzeit nicht möglich, aber könnte in ferner Zukunft möglich sein.
- Was bedeutet die „Modellierung“ einer Krankheit und warum brauchen wir sie?
- Menschliche Zellen in der Modellierung von Krankheiten
- Wie können Stammzellen bei Krankheitsmodellierungen helfen?
- Die Verwendung von iPS-Zellen als Modellsysteme für Erkrankungen
- Herausforderungen von iPS-Krankheitsmodellierungen
- Entwicklung von zukünftigen Therapien
- Erfahren Sie mehr
- Find out more (English)
- Danksagungen und Quellenangaben
Es existieren viele und verschiedenartigste menschliche Erkrankungen; einige kosten Leben, andere sind nur eine kleine Unannehmlichkeit. Ob lebensgefährlich oder nicht, eine Krankheit kann oft behandelt werden, wenn wir ihre biologische Basis verstehen. Jedoch ohne diese Basis, ist es schwer Behandlungsmethoden zu entwickeln.
Die Modellierung von Krankheiten erlaubt Wissenschaftlern bestimmte Aspekte im Labor zu untersuchen und nicht direkt am Patienten.. Ein „Krankheitsmodell“ repräsentiert die veränderte menschlichen oder tierische Biologie, die in einer spezifischen Erkrankung vorliegt. Das Modell kann zum Beispiel eine Maus mit menschlichen Krankheitssymptomen sein, oder erkrankte Zellen in einer Schale. Was auch immer es für ein Modell ist, es muss Aspekte oder die gesamte Symptomatik einer Krankheit außerhalb des menschlichen Körpers nachbilden.
Modelle ermöglichen genauere und umfangreichere wissenschaftliche Einblicke in Erkrankungen. Sie erlauben es Experimente relativ einfach zu wiederholen, was absolut notwendig ist, um Ergebnisse als vertrauenswürdig zu etablieren. Biologische Systeme wie unsere Körper sind sehr komplex und unser Verständnis ist nach wie vor sehr begrenzt. Dies führt oft zu größeren Schwankungen zwischen individuellen Experimenten, die jedoch nach vielen Wiederholungen einen eindeutigen Trend erkennen lassen. Je besser die Erkrankungen verstanden werden, desto mehr können die Experimente gezielte Fragen beantworten.
Ein erster Schritt um komplexe Erkrankungen zu studieren ist es individuelle Zellen oder Gruppen von Zellen im Labor zu analysieren, anstatt komplexes Gewebe oder den ganzen Körper zu betrachten.
Tiermodelle, wie z.B. die Labormaus, sind in der Forschung weitgehend etabliert, denn sie können viele menschlichen Krankheitssymptome nachbilden. Nichtsdestotrotz können Tiere niemals alle Aspekte der menschlichen Biologie oder Erkrankung nachbilden. Behandlungsmethoden die in experimentellen Tiermodellen effektiv waren können wesentliche Hinweise und Informationen liefern, aber funktionieren nicht immer im Menschen. Es kommt hinzu, dass Tierexperimente teuer sind und immer ethisch hinterfragt werden müssen. Krankheitsmodelle basierend auf menschlichen Zellen können diese Probleme minimieren. Die Verwendung von diesen Zellen vermeidet die Schwierigkeiten bei der Vergleichbarkeit zwischen Tier und Mensch, da hier menschliche Zellen analysiert werden.
Menschliche Zellen wurden erstmals im 19. Jahrhundert im Labor kultiviert. Seitdem, ist unser Verständnis von Zellen stark fortgeschritten. Technologische Fortschritte machten es leichter menschliche Zellen außerhalb des schützenden Körpers am Leben zu erhalten, wobei besonders Krebszellen signifikant zu diesem Prozess beigetragen haben. Krebszellen, verglichen mit gesunden Zellen, können über wesentlich längere Perioden wachsen, solange die richtigen Nährstoffe zur Verfügung stehen. Gesunde Zellen haben hingegen eine eingeschränkte Lebensspanne und sind oft viel schwieriger im Labor zu erhalten oder zu vermehren. Außerdem ist es schwierig an gesunde Kontrollzellen zu kommen, denn während einige Zelltypen, wie Haut oder Blutzellen, relativ einfach von einem Patienten entnommen werden können, sind andere, z.B. Hirnzellen, weit schwerer oder gar unmöglich zu bekommen. Eine Quelle für solche Zellen könnte also völlig neue Forschungsmöglichkeiten bieten.
Stammzellen können sich selbst regenerieren (sich selbst kopieren) und in mehr spezialisierte Zellen differenzieren (verändern). Induzierte pluripotente Stammzellen, oder kurz iPS Zellen, sind ein neuer Typ von Stammzellen, vergleichbar mit embryonalen Stammzellen, die das Modellieren und Studieren von Krankheiten momentan revolutionieren. Diese Stammzellen werden aus spezialisierten Zellen, wie Hautzellen, im Labor gewonnen und können in alle Zelltypen des Körpers differenzieren. Das bedeutet sie sind eine Quelle für bisher nur schwer oder gar nicht zugängliche Zellen, wie z.B. Hirnzellen. Um diese Fähigkeit der Differenzierung vollständig nutzen zu können arbeiten Forscher nun fieberhaft daran spezifische Zelltypen nach Bedarf zu gewinnen.
Embryonale Stammzellen, die aus 3-5-Tage alten Embryos gewonnen werden, die Fähigkeit in alle verschiedenen Zellen eines Körpers zu differenzieren. iPS-Zellen haben diesen gegenüber einen einzigartigen Vorteil für die Modellierung von Krankheiten: sie können von den Hautzellen eines Patienten gewonnen werden und sind somit patientenspezifische körpereigene Zellen. Wenn also die Krankheit eines Patienten eine genetische Ursache hat, tragen die im Labor gezüchteten iPS-Zellen den gleichen genetischen Defekt.
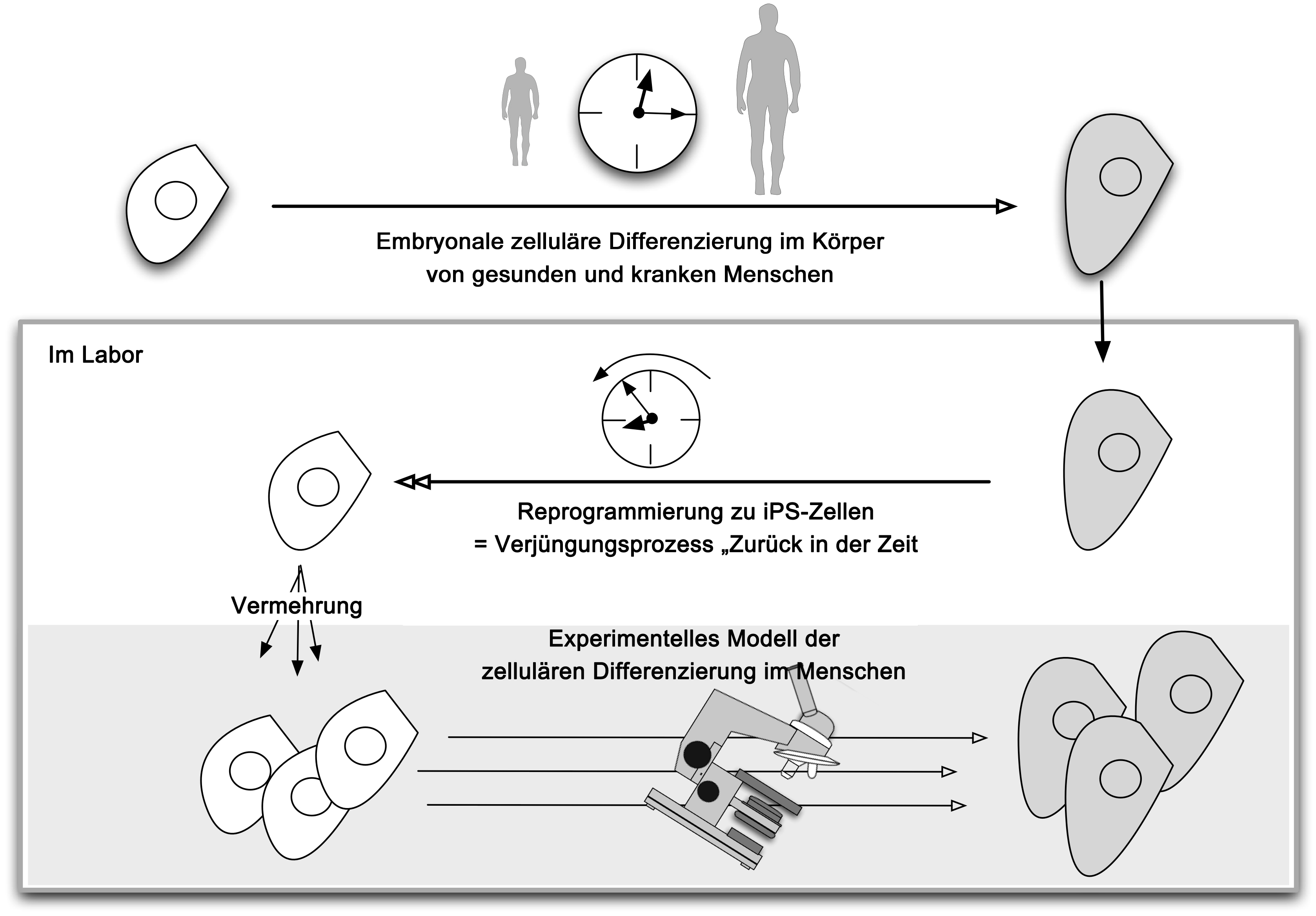
iPS-Zellen haben außerdem noch einen weiteren Vorteil. Viele Erkrankungen werden oft erst entdeckt wenn Symptome auftreten, was lange nach dem Ausbrechen der Krankheit der Fall sein kann. Die ursprüngliche Entstehung der Krankheit ist daher oft nur schwer zu verfolgen und zu verstehen. Durch die Reprogrammierung von iPS-Zellen werden jedoch alternde Zellen verjüngt, wobei man erwachsene Zellen, wie Hautzellen, in ihr frühes embryonales Stadium zurückverwandelt. Diese iPS-Zellen können dann von Forschern genutzt werden um jede Art Zelle, ob aus einem frühen oder späten Zellentwicklungsstadium zu gewinnen. Dies gibt Wissenschaftlern die Möglichkeit Ereignisse zu modellieren, die in einem erkrankten Körper vor langer Zeit stattgefunden haben.
In den letzten Jahren wurden iPS-Zellen von Patienten mit verschiedensten Erkrankungen gewonnen. Ein Beispiel für die Verwendung von iPS-Krankheitsmodellen ist die Forschung an der momentan unheilbaren Krankheit, Spinale Muskelatrophie (SMA). SMA Patienten haben einen spezifischen Defekt in einem Gen, genannt SMN1. Dieser genetische Fehler beeinträchtigt Nervenzellen im Rückenmark, was in Muskelschwäche, schwerer Behinderung und kürzerer Lebenszeit bei Kindern endet. Während die betroffenen Nervenzellen sehr schwer von Spendern zu bekommen sind, ist es möglich sie von iPS-Zellen zu gewinnen. SMA-iPS-Zellen ohne ein arbeitendes SMN1 Gen wurden als Modell verwendet um den Ursprung der Erkrankung in sich neu entwickelnden Nervenzellen zu studieren. Diese SMA-iPS-Zellen erlauben daher die Entwicklung neuer Behandlungsmethoden ohne die Notwendigkeit für Tests direkt am Patienten in der frühen Phase der Entwicklung.
Außer der Spinalen Muskelatrophie (SMA) sind eine Reihe von anderen Erkrankungen mit iPS-Zellen untersucht worden. Hierzu gehören amyotrophe Lateralsklerose (ALS), Alzheimer-Krankheit, Ataxia teleangiectatica (Louis-Bar-Syndrom), Down-Syndrom, familiäre Dysautonomie, Fragile-X-Syndrom, Friedrich-Ataxie, Huntington-Krankheit, Niemann-Pick Krankheit, Parkinson-Krankheit und Schizophrenie. Krankheitsmodelle, die iPS-Zellen verwenden, sind auch für viele andere neurologische, metabolische, kardiovaskuläre und Immunschwäche-Erkrankungen sowie für Erkrankungen des Blutsystems in der Entwicklung. Die Anzahl der auf diese Weise untersuchten Krankheiten nimmt stetig zu.
Ein bemerkenswertes Beispiel dafür, wie ein iPS-Zell-basierte Modelle verwendet werden, um eine Krankheit zu untersuchen und eine potenzielle Heilung zu entdecken, ist eine Reihe neuester Studien zur amyotrophen Lateralsklerose (ALS). ALS- oder Lou-Gehrig-Krankheit ist eine tödliche Erkrankung, die zu Muskelschwund und Lähmung aufgrund des Verlustes von Nervenzellen im Rückenmark führt. Mutationen im Gen SUPEROXID DISMUTASE 1 (SOD1) verursachen etwa ein Viertel der erblichen Formen von ALS. Es gibt derzeit keine Heilung für diese verheerende Krankheit und das einzige Medikament, das für ALS-Patienten verfügbar ist, ist Riluzol, das lediglich den Beginn einiger Aspekte der Krankheit verzögert. Die Entdeckung neuer Medikamente für ALS wurde durch den Mangel an geeigneten Modellen für die präklinische Prüfung potenzieller Medikamente erschwert. Die gegenwärtigen Tiermodelle mit Nagetieren zu ALS stellen den Phänotyp der menschlichen Krankheit nicht vollständig dar. Vor kurzem haben Forscher iPS-Zellen von ALS-Patienten erzeugt und diese verwendet, um die ALS-Nervenzellen zu produzieren. Diese Nervenzellen zeigten ALS-typische Krankheitseigenschaften und wurden verwendet, um nach Medikamenten zu suchen, die die Krankheit lindern könnten. Ein solches Medikament, Ezogabin, wird derzeit in klinischen Studien getestet. Die Hoffnung ist, dass die klinischen Studien erfolgreich sind und ALS-Patienten geheilt werden könnten. Selbst wenn die Studie keinen Erfolg bringt, haben Forscher nun ein wertvolles Modell, um die Krankheit weiter zu untersuchen und neue potenzielle Medikamente zu testen.
iPS-Zellen sind vielversprechend und werden nun in vielen Forschungsinstituten gewonnen. Man muss sich allerdings bewusst sein, das diese neue Technologie auch ihre Probleme mit sich bringt und nicht alle wissenschaftlichen Fragestellungen beantworten kann.
- Ein neuer Typ von Stammzellen– iPS-Zellen sind ein komplett neuer, im Labor gezüchteter Typ von Stammzellen. Mehr Forschung ist notwendig um den Reprogrammierungsprozess und seinen Effekt auf die Zellen, inklusive Nutzen und Risiken, zu verstehen.
- Das Nachbilden einer Krankheit ist komplex – Krankheitsmodellierung durch iPS-Zellen findet außerhalb des Körpers statt und basiert auf Fehlern in der DNA. Obwohl Krankheiten oft vollständig oder teilweise durch Fehler im DNA Code entstehen, können auch andere biologische Prozesse Erkrankungen beeinflussen oder auslösen. Einige von diesen DNA-unabhängigen Krankheitsprozessen können nicht einfach mit der aktuellen iPS Zelltechnologie kontrolliert oder wiedergespiegelt werden. Dennoch, können iPS Krankheitsmodelle zumindest helfen aufzuschlüsseln ob DNA-abhängige oder DNA-unabhängige Prozesse eine Rolle spielen.
- Krankheitsmodelle für verschiedene Arten von Krankheiten - Obwohl iPS-Zellen theoretisch als Modell für jede Erkrankung verwendet werden könnten, eignen sie sich besser für die Modellierung von Krankheiten, die durch Mutationen in einem einzigen Gen (monogene Erkrankungen) verursacht werden, als für die Modellierung von Krankheiten, die durch Veränderungen mehrerer Gene entstehen (polygene oder komplexe Krankheiten) oder Krankheiten, die durch Umweltfaktoren verursacht werden.
- Krankheiten beeinflussen oft viele Zelltypen– Krankheitsmodelle mit iPS-Zellenerlauben es zu erforschen wie spezifische Zellen von einer Krankheit beeinträchtigt werden. Jedoch befallen viele Erkrankungen komplexe Gewebe oder Organe die verschiedene Arten von Zellen in vielen miteinander interagierenden Schichten beinhalten. Die Interaktion zwischen verschiedenen Zellen ist oft zumindest teilweise für die Auswirkungen einer Krankheit verantwortlich. Forscher beginnen nun, komplexere Systeme zu erschaffen um diese Aspekte von Krankheiten komplett modellieren zu können. Ein Ansatz benutzt Stammzellen, um Zellgruppen in 3D Strukturen, die Gewebe verschiedener Organe aehneln, wachsen zu lassen. Das Wachsen und die Nutzung dieser ‘Organoide’ steckt noch in den Kinderschuhen und erfordert fortgeschrittende 3D Differenzierungstechnologien. Wenn diese Methoden jedoch einmal etabliert sind, koennten Organoide als komplexe Krankheitsmodelle benutzt werden, besser als es flache (2D) Zellkulturmodelle schaffen.
iPS-Zellen geben Forschern die Möglichkeit vorher schwer erreichbare „kranke“ menschlichen Zellen, wie z.B. Hirnzellen, zu studieren. Ihr Nutzen für die Modellierung von Krankheiten ist ein Meilenstein für das bessere Verständnis von vielen Krankheiten. Weiterhin können diese Krankheitsmodelle mit iPS-Zellen dazu genutzt werden um Medikamente und Behandlungsmethoden direkt am „Zellpatienten“ zu entwickeln und testen.
Dieses Factsheet wurde erstellt von Christian Unger. Es wurde geprüft und erneuert 2013 von Peter Andrews, 2016 von Ivana Barbaric und 2018 von Paul Gokhale.
Die Animation wurde von Duncan Brown erstellt.
Übersetzung ins Deutsche von Wolfgang und Christian Unger.
Das Hauptbild wurde von Emma Kemp mithilfe von Servier Medical Art erstellt. Foto mit Pillen von MorgueFile. Andere Bilder von Christian Unger.