Leukämie: wie können Stammzellen helfen?
Leukämie war die erste Erkrankung, bei der transplantierte Blutstammzellen als Therapie eingesetzt wurden und in vielen Fällen eine Heilung ermöglichten. Heute erhalten tausende Patienten mit Leukämie auf der ganzen Welt diese Therapie. Aber noch sind nicht alle Schwierigkeiten beseitigt. Die aktuelle Forschung versucht unser Verständnis für viele Krebserkrankungen des blutbildenden Systems zu erweitern und Therapien zu optimieren. Was sind die neuesten Fortschritte und welche Herausforderungen verbleiben noch?
Was wissen wir? ▼
Leukämie ist der Hauptbegriff fuer viele verschiedene Blutkrebsarten mit unterschiedlichen Ursachen, Therapien und Heilungschancen. Akute Leukaemien haben ungewoehnlich erhoehte Blutzellen, die nicht richtig funktionieren und oft die Bildung normaler Blutzellen unterdruecken.
Die aktuellen Stammzelltherapien bei schwerer Leukämie umfassen u. a. die Blutstammzelltransplantation (auch bezeichnet als hämatopoetische Stammzell- Knochenmarks- oder Nabelschnurbluttransplantation.
Tausende Leukämie-Patienten auf der ganzen Welt wurden erfolgreich mit Blutstammzelltransplantationen therapiert. Obwohl diese Behandlungen immer noch sehr grosse Risiken bergen, sind diese im Laufe der Jahre, deutlich geringer geworden, da die Forscher immer besser über Leukämie und Blutstammzellen Bescheid wissen.
Was untersuchen Forscher? ▼
Heutzutage wissen die Forscher die meisten Genmutationen, die wahrscheinlich in den meisten Leukaemiearten vorkommen. Studien zur Untersuchung der hämatopoetischen Stammzellen (HSZ) (oder ihrer Tochterzellen) und der Auslöser für ihre Verwandlung in Blutkrebszellen laufen.
Um derzeitige Grenzen der HSZ-Transplantationen gering zu halten, untersuchen Forscher derzeit neue Ansätze, z. B. die Entwicklung von Behandlungen mit Immunzellen, Möglichkeiten zum Ankurbeln der Immunität des Patienten und Wege, um die Blutzellproduktion in mehr Patienten mit Hilfe von derzeitigen oder alternativen Quellen von Zellen fuer Transplantationen schneller wiederherzustellen. Neuere Ansaetze beinhalten Strategien, um HSZ im Labor zu vermehren oder HSZ von Zellen, den sogenannten induzierten pluripotenten Stammzellen (iPSZ) zu erhalten. Diese iPSZ sind unsterbliche Zellen, die momentan leicht im Labor hergestellt werden.
Was sind die Herausforderungen? ▼
Unmittelbar vor Durchfuehrung der Transplantation werden das Blut und Immunsystem des Patienten durch Chemotherapie weitgehend zerstört. Dadurch kann der Patient keine Infektionen abwehren, bis die transplantierten Zellen reife Zellen zur Immunabwehr wieder hergestellt haben. Eine Herausforderung besteht weiterhin darin, diese Infektionsanfälligkeit der Patienten niedrig zu halten, während die transplantierten HSZ das Immunsystem des Patienten wieder aufbauen.
Eine zweite grosse Herausforderung wird von geringen genetischen Unterschieden zwischen transplantierten HSZ und dem Patienten verursacht, selbst wenn Spender- und Patientengewebetypen weitgehend zueinander passen. Solche Unterschiede koennen unerwartete ernsthafte Inkompatibilitäten verursachen, die zur Transplantatabstoßung oder der Graft-versus-Host-Krankheit (transplantierte Zellen greifen das Patientengewebe an) führen, die in extremen Fällen tödlich verlaufen kann.
- Über Leukämie
- Was verursacht Leukämie?
- Wie werden gesunde Blutstammzellen zur Leukämietherapie verwendet?
- Die Grenzen aktueller Stammzelltherapien
- Aktuelle Entwicklungen in der Leukämie-Forschung
- Die Zukunft
- Erfahren Sie mehr
- Find out more (English)
- Danksagungen und Quellenangaben
Leukämie ist die Bezeichnung für viele verschiedene Arten von Blutkrebs. Eine Gemeinsamkeit all dieser Formen von Leukämie ist die Produktion von zu vielen weißen Blutzellen (auch Leukozyten genannt) und dass diese leukämischen Zellen nicht naturgemäß heranreifen. In den ernsthaftesten Leukaemiearten sehen diese Zellen wie normale unreife Zellen, auch Blasten genannt, aus. Da diese leukaemischen Blasten im unreifen Zustand bleiben, sind diese nicht in der Lage, die Funktionen normaler, reifer Blutzellen, die Verteidigung des Körpers gegen Infektionen und Krankheiten, auszuführen. Bei den meisten Formen akuter Leukämie sammeln sich die leukämischen Blasten im Knochenmark sowie im Blut an und unterdrücken auch die Bildung normaler Blutzellen. Die Produktion einer übermäßigen Anzahl von Blutzellen und der Verlust der Fähigkeit Infektionen zu bekämpfen sind Gründe, warum Leukämie so schnell zu einer potenziell tödlichen Erkrankung wird, wenn man sie nicht erfolgreich behandelt.
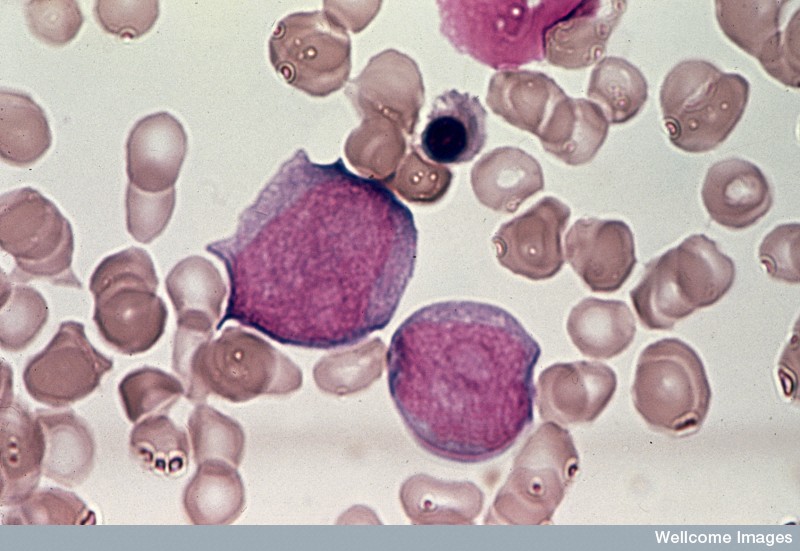
Leukämien werden nach dem Schweregrad der Erkrankung eingeteilt (wie rasch sie verläuft) und nach der Art der betroffenen weißen Blutzellen:
- Akute Leukämien sind Erkrankungen, in denen die leukaemischen Zellen sich schnell entwickeln und deswegen sofort behandelt werden müssen. Sie werden üblicherweise in akute lymphatische Leukämien (ALL) oder akute myeloische Leukämien (AML) unterteilt, je nachdem welcher Zelltyp betroffen ist.
- Chronische Leukämien sind Erkrankungen, in denen sich die leukaemischen Zellen langsamer entwickeln und eine normale Bildung von Blutzellen nicht verhindern. Deshalb koennen die Symptome milder ausfallen und die Erkrankung faellt oft über Jahre nicht auf, bis sie schlussendlich diagnostiziert werden. Chronische Leukaemien werden üblicherweise in chronische lymphatische Leukämien (CLL) oder chronische myeloische Leukämien (CML) unterteilt, je nachdem welche weissen Blutzellen betroffen sind.
- Zusaetzlich gibt es auch andere Arten und Unterarten der Leukämie: sie haben Zwischenstadien der Symptome und Pathologie.
Sowohl chronische als auch akute Subtypen der Leukämie können sich schon in der frühen Kindheit entwickeln, haben jedoch eine höhere Häufigkeit in älteren Patienten. Jedoch unterscheiden sich die Eigenschaften leukaemischer Zellen in jungen Kindern etwas von denen in Erwachsenen und deren Behandlung ist auch herausfordernder.
Wie die meisten Krebsarten wird auch Leukämie durch eine Reihe seltener Mutationen (Veränderungen) in den Genen einzelner primitiver Blutvorläuferzellen verursacht. Allgemein entstehen diese in primitiven Vorlaeufern von Blutzellen das ganze Leben lang in sehr geringer Rate. Sehr selten kann eines dieser mutierten Gene vererbt werden und dann eine genetisch bedingte hohe Anfälligkeit für die Ausbildung von Leukämie bei der jeweiligen Person bewirken. Andere bekannte aber auch seltene Ursachen sind zum Beispiel radioaktive Strahlung oder vorhergehende Einnahme gewisser Medikamente zur Krebsbehandlung. Es wird angenommen, dass eine voll ausgeprägte Leukämie erst auftritt, wenn gewoehnlich verschiedene Mutationen zusammentreffen und dadurch die für die normale Bildung von Blutzellen verantwortlichen molekularen Programme dauerhaft verändert werden.
Eine große Anzahl von Genmutationen sind mittlerweile als Ursache fuer humane Leukämie in Verbindung gebracht worden. In einigen Fällen ist es immer wieder dieselbe Mutation, die konstant zu einem bestimmten Leukämie Typus zu führen scheint. CML ist ein Beispiel für eine Leukämie, bei der das Wissen um solch eine Mutation die Entwicklung eines darauf zugeschnittenen Medikaments (Gleevec) ermöglicht hat, das sehr erfolgreich und spezifisch die leukämischen Zellen in Patienten, die mit einem fruehen Stadium (chronische Phase) der CML diganostiziert wurden, abtötet. In den meisten Fällen anderer Leukaemien jedoch stellt die Vielfalt der in den Zellen vorherrschenden Mutationen die Entwicklung wirkungsvoller “gerichteter” Therapien eine groessere Herausforderung dar.
Weil viele Leukämien ihren Ursprung in mehrfachen seltenen Mutationen haben, nimmt man an, dass die erste Veränderung in eine Zelle stattfindet, die eine lange Zeit im Körper verbleiben kann. Ein Hauptkandidat für diese Art von Zellen sind daher die einfachsten Blutvorläuferzellen – auch hämatopoetische Stammzellen (HSZ) genannt. HSZ sind dafür verantwortlich, über die gesamte Lebenszeit neue Blutzellen im Körper zu produzieren. Wenn eine Stammzelle von einer genetischen Veränderung betroffen ist, erben auch alle von ihr abstammenden Zellen, dieselbe Mutation. Es wurde gezeigt, dass CML mit einer besonderen Mutation in einer HSZ beginnt. Die Tochterzellen der ersten Zellen, die mutiert wird, müssen dann jedoch eine Anzahl von Schritten durchlaufen um sich in reife weisse Blutzellen zu verwandeln. Die Entstehung neuer Mutationen kann an jedem dieser Schritte auftreten.
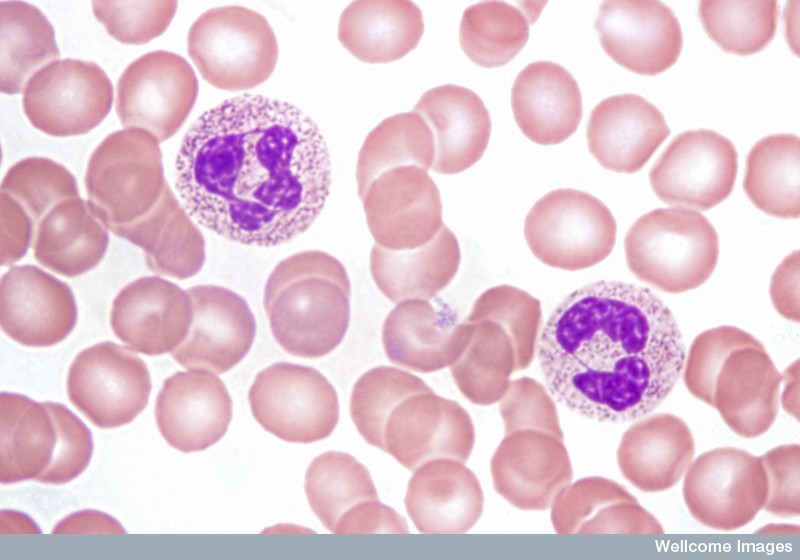
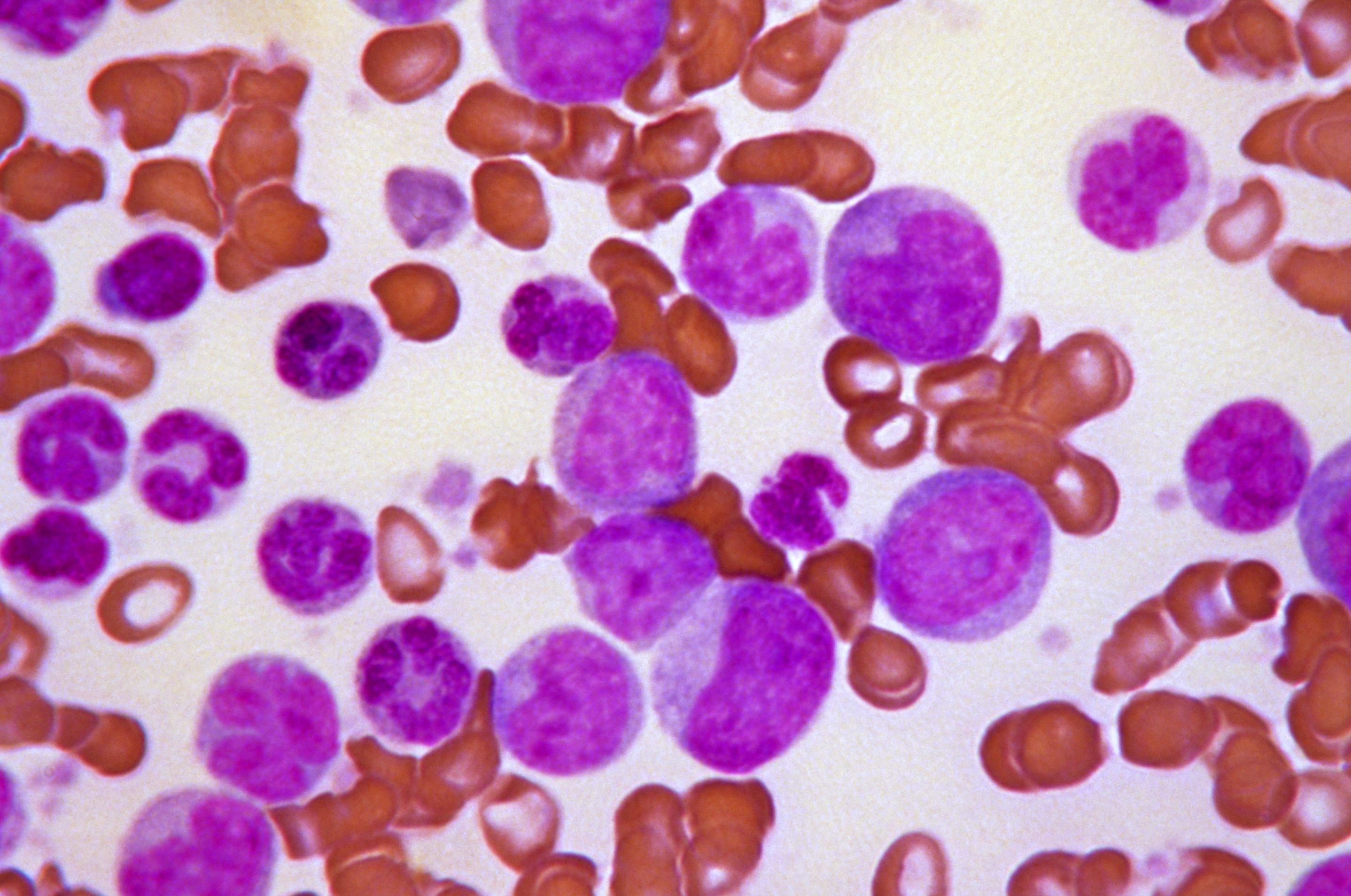
Akute Leukämien benoetigen normalerweise sofortige und intensive Behandlung. Je nach Art von Leukämie und Zustand des Patienten umfassen Behandlungsmethoden unter anderem Chemotherapie, Steroide oder aufwendigere Verfahren wie hochdosierter Chemotherapie und einer darauf folgenden Transplantation gesunder HSZ.

Hochdosierte Chemotherapie ist die derzeit effektivste Methode leukämische Zellen abzutöten und sie kann einige Patienten dauerhaft heilen. Allerdings schädigt sie auch die verbleibenden blutproduzierenden Zellen im Knochenmark. Um diese Zellen zu ersetzen, erhalten die Patienten ein Transplantat, das sowohl HSZ als auch andere wichtige Zellen, die zur Behandlung beitragen, enthaelt.. Die Zellen für das Transplantat können vom Blut oder Knochenmark eines gesunden Spenders gewonnen werden. Solche Transplantate sind wirkungsvoll, da sie neben verschiedener Untergruppen von HSZ auch wichtige Immunzellen enthalten, die dabei helfen verschieden schnell leukaemische Zellen zu beseitigen und die Blutproduktion wiederherzustellen. Auch die Zellen des Patienten selbst können manchmal für die Transplantation verwendet werden – vorausgesetzt es ist möglich, genügend gesunde Zellen zu sammeln bevor die Transplantation stattfindet. Sollte ein fremder Spender benötigt werden, müssen gewisse Gewebemerkmale mit denen des Empfängers übereinstimmen, um das Risiko einer Abstossung des Transplantats zu reduzieren.
Intensive Chemotherapie mit darauffolgender HSZ Transplantation ist weiterhin eine der wirkungsvollsten Methoden der Behandlung vieler Arten der akuten Leukämie. Allerdings ist die Behandlungsmethode risikoreich, mit der Möglichkeit beträchtlicher Nebenwirkungen, erhöhter Sterblichkeit und ausgeprägten Nachwirkungen in Langzeit-Überlebenden, insbesondere bei Kindern. Deshalb wird diese Art der Therapie nur angewendet, wenn hervorragend passende Spenderzellen zur Verfuegung stehen und die Krankheitsmerkmale zur Gruppe mit schlechter Prognose gehoeren.
Trotz des großen Erfolgs von hämatopoetischen Stammzelltransplantationen kann die Verwendung von fremden Spender-Zellen auch erhebliche Nebenwirkungen aufweisen:
Infektionen – Transplantierte HSZ brauchen Zeit um neue Blutzellen herzustellen, die fuer die wirkungsvolle Abwehr von Infektionen benoetigt werden, selbst wenn Wachstumsfaktoren verabreicht werden, die diesen Vorgang beschleunigen. Der Patient ist daher während dieser Zeit anfälliger für Infektionen aufgrund der verzögerten Wiederherstellung des Immunsystems. Sorgfältige Beobachtung, beschränkter Umgang mit anderen Personen und vorbeugende Behandlung mit Antibiotika können dabei helfen, das Infektionsrisiko zu senken.
Graft-versus-Host-Reaktion (auch: Transplantat-Wirt-Reaktion, GvHR) – Diese Komplikation tritt auf wenn Spenderzellen das Gewebe des Patienten angreifen. Symptome umfassen Hautausschläge, Durchfall, Blasen und Fieber. Die Graft-versus-Host-Reaktion ist eine sehr schwerwiegende Komplikation und kann lebensgefährlich sein. Das Risiko, eine GvHR zu entwickeln, ist geringer je ähnlicher die Gewebsmerkmale der Zellen des Spenders denen des Empfängers sind – das heißt je kompatibler der Spender ist. Daher sind Geschwister als Spender am besten geeignet. Andere Strategien versuchen, die GvHR zu verhindern, indem sie das Immunsystem des Patienten mit Medikamenten unterdrücken oder gewisse weisse Blutzellen (Lymphozyten) aus dem urspruenglichen Transplantat entfernen bevor sie es für den Patienten verwenden. Jedoch weiss man jetzt, dass transplantierte Immunzellen auch eine wichtige Rolle bei der Ausloeschung der leukaemischen Zellen von Patienten spielen. Folglich liegt die Herausforderung darin, ein nuetzliches Gleichgewicht zwischen einem wirkungsvollen Graft-versus-Leukaemie (GvL) und geringem GvHD Effekt zu erringen.
Wissenschaftler und Mediziner untersuchen verschiedene Wege aktuelle Transplantationsmethoden zu verbessern um diese Limitationen zu beseitigen. Eine weitere Herausforderung ist der Mangel an kompatiblen Spendern. Verschiedene Organisationen arbeiten daran, die Anzahl registrierter freiwilliger Spender zu erhöhen.
Hochdosierte Chemotherapie, mit der Patienten vor der Verabreichung eines Transplantats behandelt werden, zerstört nicht nur bösartige leukämische Zellen sondern auch gesunde Knochenmarkszellen. Neuartige Formen der Transplantation – auch mini-Allo(Fremd)transplantate oder reduzierte Intensitäts-Allotransplantate genannt – wurden entwickelt um Auswirkungen auf normale Zellen zu mindern und den GvL Effekt auf das Transplantat zu verstaerken. Diese Behandlungsmethoden ermöglichen eine Dosissenkung bei der Chemotherapie, die dabei hilft, einen zu großen Schaden am Knochenmark zu vermeiden. Dann werden Spenderimmunzellen mit den Spenderblutzellen mittransplantiert, welche die verbleibenden leukämischen Zellen des Patienten angreifen und beseitigen. Diese Art von Transplantation ist weniger aggressiv und weist weniger Nebenwirkungen auf als andere, allerdings verbleiben auch hier einige ernste Risiken wie zum Beispiel die GvHR.
Derzeit werden zahlreiche neue Methoden die helfen sollen GvHR zu vermeiden, in der Klinik getestet. Spezielle Immunzellarten (regulatorische T-Lymphozyten), die eine unterdrückende Wirkung auf das Immunsystem ausüben, können verabreicht werden. Dies soll die Spenderimmunzellen davon abhalten, das Gewebe des Patienten anzugreifen. Alternativ gibt es auch Versuche, selektiv all jene Immunzellen vom urspruenglichen Transplantat zu entfernen welche die GvHR hervorrufen können. Die Erzeugung genetisch veraenderter Immunzellen, die speziell die Leukaemiezellen der Patienten (besonders lymphoide Leukaemien) abtoeten, ist momentan in der Klinik vielversprechend.
Des weiteren wird an Möglichkeiten geforscht, die Zeit bis zur vollständigen Regeneration des Immunsystems des Patienten nach einem Stammzelltransplantat zu verringern. Patienten bekommen nun routinemaessig gewisse ausgewaehlte Proteine, auch Wachstumsfaktoren genannt, die speziell die Produktion von Zellen steigern, die dabei helfen Infektionen abzuwehren. Auch dies kann das Infektionsrisiko für den Patienten während der Genesung mindern. Ein weiterer aktiver Wissenschaftsbereicht ist die Entwicklung neuer Methoden, um HSZ im Labor zu vermehren. Diese Strategie ist von besonderem Interesse um zu ermoeglichen, dass Blutzellen der Nabelschnur von Geburten auf der ganzen Welt gesammelt und eingefroren werden. Diese Zellen haben sehr wirkungsvolle regenerative Eigenschaften. Jedoch kommen sie in zu geringer Anzahl in Erwachsenen vor, um verbreitet nuetzliche zu sein, es sei denn, sie werden zusammen mit mehreren Sammlungen gegeben.
Die Stammzellforschung ist ein rasch voranschreitendes Fachgebiet. Neue Technologien, wie zum Beispiel die Herstellung induzierter pluripotenter Stammzellen (IPS) oder HSZ durch Umwandlung anderer Zelltypen in HSZ werden heute schon entwickelt und im Labor benutzt, um zu untersuchen, wie normale menschliche HSZ aufrechterhalten werden und wie menschliche Leukaemie entsteht. Diese Studien liefern voraussichtlich neue Informationen ueber diese Zellen und wie man neue, moeglicherweise wirkungsvollere und weniger schaedliche Therapien plant und testet. Solch Forschung könnte dabei helfen, den Mangel an Knochenmarksspendern und die Schwächen derzeitiger Transplantationsmethoden auszugleichen.
EuroStemCell factsheet: Blutstammzellen
Stammzellen aus Nabelschnurblut: heutige Verwendung und künftige Herausforderungen
Informationsseite des Deutschen Krebsforschungszentrums (dkfz)
Informationsseite der Schweizer Krebsliga
Informationsseite der Deutschen Krebsgesellschaft
Video from Nature on leukaemia: discovery, how it works and current research (6 mins)
World Marrow Donor Association
Center for International Blood and Bone Marrow Transplantation Research
Anthony Nolan Foundation bone marrow donor registry UK
US National Marrow Donor Program
The European Group for Blood and Bone Marrow Transplantation
UK National Health Service information on bone marrow transplants
Dieses Factsheet wurde erstellt von Christine Weber.
Geprüft 2013 von Connie Eaves und Linda Barber.
Geprueft und aktualisiert 2015 und 2018 von Connie Eaves.
Übersetzung ins Deutsche von Christine Weber und Christina Schoenherr.
Bildquellen:
Blut bei chronischer myeloischer Leukämie von Junia Melo/Wellcome Images.
Gesundes Blut von Spike Walker/Wellcome Images.
Blastenkrise bei chronischer myeloischer Leukämie von CDC/ Stacy Howard.
Blutprobe bei Akuter Leukämie von Wellcome Images.
Leukämie Patienten die Prozeduren der Chemotherapie demonstrieren von Bill Branson.